تعریف ایزوتوپ:
به اتم های یک عنصر که عدد اتمی یکسان ولی عدد جرمی متفاوت دارند، ایزوتوپ می گویند.
نام دیگر ایزوتوپ چیست؟
ایزوتوپ ها را هم مکان می نامند. چرا که همگی در یک مکان یا خانه از جدول تناوبی قرار می گیرند.
مقایسه ایزوتوپ های یک عنصر:
تمام ایزوتوپ های یک عنصر، پروتون های برابر دارند و پروتون ها تعیین کننده خواص شیمیایی عناصر هستند. از این رو می توان گفت که ایزوتوپ های یک عنصر خواص شیمیایی یکسانی دارند ولی از نظر خواص فیزیکی وابسته به جرم مثل دمای ذوب و جوش و چگالی متفاوت اند.
چند مثال از ایزوتوپ های طبیعی عناصر:
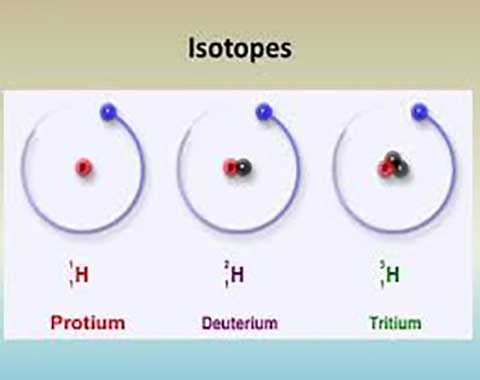
- هیدروژن عنصری با سه ایزوتوپ می باشد. عدد اتمی هر سه ۱ و عدد جرمی آن ها به ترتیب ۱،۲و ۳ است.
- کربن عنصری با سه ایزوتوپ می باشد. عدد اتمی هر سه ۶ و عدد جرمی آن ها به ترتیب ۱۲،۱۳ و ۱۴ است.
- منیزیم عنصری با سه ایزوتوپ می باشد. عدد اتمی هر سه ۱۲ و عدد جرمی آن ها به ترتیب ۲۴، ۲۵ و ۲۶ است.
- لیتیم عنصری با دو ایزوتوپ است. عدد اتمی هر دو ۳ و عدد جرمی آن ها به ترتیب ۶ و ۷ میباشد.
- کلر هالوژنی با دو ایزوتوپ است. عدد اتمی هر دو ۱۷ و عدد جرمی آن ها ۳۵ و ۳۷ است.
انواع ایزوتوپ ها:
ایزوتوپ ها بر اساس تعداد پروتون ها و نوترون هایی که دارند به دو دسته کلی زیر تقسیم می شوند:
- ایزوتوپ های پایدار
- ایزوتوپ های ناپایدار
ایزوتوپ های پایدار:
در صورتی که نسبت تعداد نوترون ها به پروتون های یک ایزوتوپ کمتر از ۱٫۵ باشد، آن ایزوتوپ پایدار است.
استثنای این قانون، ایزوتوپ عنصر تکنسیم با عدد اتمی ۴۳ و عدد جرمی ۹۹ است. نسبت تعداد نوترون ها به پروتون ها در این ایزوتوپ، کمتر از ۱٫۵ است اما ایزوتوپی ناپایدار محسوب می شود.
ایزوتوپ های ناپایدار:
در صورتی که نسبت تعداد نوترون ها به پروتون های یک ایزوتوپ برابر یا بیش از ۱٫۵ باشد، آن ایزوتوپ ناپایدار محسوب می شود.
استثنای این قانون ایزوتوپ عنصر اورانیوم می باشد که عدد اتمی ۹۲ و عدد جرمی ۲۳۸ دارد. نسبت تعداد نوترون ها به پروتون ها در این ایزوتوپ، بالای ۱٫۵ است اما ایزوتوپی پایدار محسوب می شود.
ایزوتوپ های ناپایدار پرتوزا هستند و هسته آن ها به مرور زمان متلاشی می شود و انرژی زیادی آزاد می کند.
محاسبه درصد فراوانی ایزوتوپ ها:
برای محاسبه درصد فراوانی یک ایزوتوپ می توان از فرمول زیر استفاده کرد.
توجه داشته باشید که مجوع درصد فراوانی همه ی ایزوتوپ های یک عنصر مساوی با ۱۰۰ می باشد.
مثلا از همه اتم های لیتیم که در طبیعت دیده می شود، ۹۴ درصد آن ها ایزوتوپی با عدد جرمی ۷ و تنها ۶ درصدشان ایزوتوپی با عدد جرمی ۶ هستند
منبع : http://elmnama.com
تهیه کننده : رمضان حبیبی ( دبیر علوم تجربی )
تایید کننده : رسول سمیعی ( معاون آموزشی دبیرستان )